INTRODUÇÃO
A cirurgia cardíaca com circulação extracorpórea (CEC) representou uma das grandes conquistas médicas do século XX, porém, um dos efeitos colaterais indesejáveis após sua utilização é a insuficiência renal, que pode ocorrer por diversos fatores, sendo muitas vezes mais acentuada nas crianças no período neonatal [1,2].
Quando uma criança é submetida a correção de defeito cardíaco congênito com CEC e evolui com insuficiência renal, pode ser tratada por diálise peritoneal [3,4]. Durante a realização da diálise, a solução é introduzida no abdome por um cateter inserido na região peritoneal e, após um determinado tempo o líquido é drenado, reiniciando assim um novo ciclo [5,6].
A peritonite é complicação frequente nos pacientes em diálise peritoneal e continua sendo importante causa de morbidade e abandono da técnica nos doentes em tratamento [7,8]. O risco para o desenvolvimento de peritonite deve-se a diversos fatores, tais como, tempo prolongado de tratamento, velocidade das trocas dos banhos, concentrações das soluções e o uso do cateter, o qual mantém a continuidade do peritônio com o meio externo [8].
Embora já existam técnicas automatizadas para diálise peritoneal, a forma manual é muito utilizada em hospitais de países em desenvolvimento, devido à simplicidade de manuseio das trocas de banho e a suavidade do próprio processo [9,10].
Para o procedimento, há disponível no mercado brasileiro apenas um sistema de diálise peritoneal neonatal capaz de controlar o volume de líquido a ser infundido e que exige adaptadores específicos para sua utilização [11]. Na maioria dos serviços, o sistema de diálise peritoneal é confeccionado manualmente pela conexão de vários circuitos independentes, projetados para outras finalidades. Este manuseio facilita a ocorrência de falhas na montagem, com conseqüente aumento do risco de infecção, em especial a peritonite [8].
Com esta preocupação, o objetivo do estudo foi desenvolver um novo sistema de diálise peritoneal pediátrico totalmente fechado, de fácil manejo e avaliar o nível de garantia de esterilidade.
MÉTODOS
No período de fevereiro a dezembro de 2008, foi desenvolvido e testado, em parceria com o Setor de Bioengenharia da Braile Biomédica Indústria, Comércio e Representações S/A®, um sistema de diálise peritoneal pediátrico totalmente fechado.
O sistema fechado é constituído por duas vias, a de infusão da solução e a de drenagem, bastando apenas duas conexões para o estabelecimento da diálise peritoneal (Figura 1). É composto por tubos, conectores e reservatórios de policloreto de vinila (PVC), conectados e colados com solvente ciclohexanona.
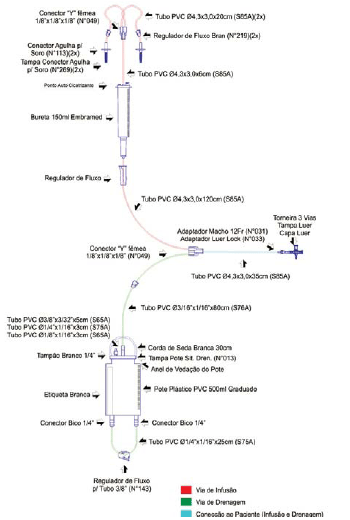
Fig. 1 - Esquema do sistema de diálise peritoneal pediátrico fechado. Observam-se os componentes e suas respectivas dimensões. PVC = Policloreto de vinila
Foram montados 20 sistemas de diálise peritoneal pediátrico, acondicionados separadamente em dupla embalagem plástica e caixa de papelão. Os sistemas foram esterilizados em gás óxido de etileno (ETO) na concentração de 592 mg, pressão a vácuo de - 0,65 kg/cm
2 e pressão de trabalho de + 0,42 kg/cm
2 por 4 horas. Após a esterilização, foram divididos em dois grupos, de acordo com o teste aplicado:
Grupos A (n=10) - sistemas submetidos ao teste de esterilidade; Grupo B (n=10) - sistemas submetidos ao teste de penetração de gás.
O teste de esterilidade (Grupo A) foi realizado no Laboratório de Microbiologia, em área classificada e consistiu na lavagem de todo o sistema com 120 ml de solução fisiológica 0,9% que, em seguida foi coletada nas saídas das vias de infusão (60 ml) e drenagem (60 ml). Esta solução foi filtrada em membrana de 0,45µm e incubada em dois meios de cultura diferentes, um para bactérias e outro para fungos. Para análise e leitura dos resultados, os sistemas foram sequencialmente identificados de S1 a S10. Como controle positivo, os meios de cultura foram submetidos ao teste de promoção de crescimento (
Growth Promotion Test), com inoculação de cepas.
O teste de penetração de gás (Grupo B) foi realizado por meio dos indicadores químicos distribuídos no sistema como demonstrado na Figura 2. Após esterilização, os 10 sistemas foram destruídos para remoção dos indicadores e identificados sequencialmente por S11.1 a S20.5.
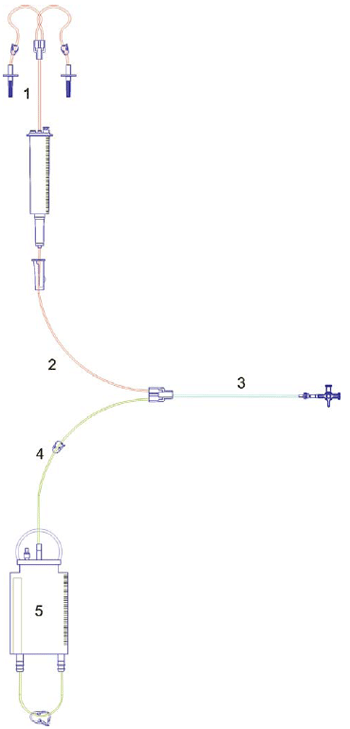
Fig. 2 - Esquema do sistema de diálise peritoneal pediátrico fechado indicando os locais em que foram inseridos os indicadores químicos
O resultado do teste de esterilidade (Grupo A) de todas as membranas foi negativo para bactérias e fungos.
No teste de penetração do gás ETO (Grupo B), observou-se alteração de cor em todos os indicadores químicos.
DISCUSSÃO
O novo sistema de diálise peritoneal pediátrico fechado, que requer manipulações mínimas, poderá diminuir os riscos de peritonites, quando aplicado em pacientes. Na literatura há trabalhos demonstrando aumento do índice de infecção abdominal em pacientes que utilizaram sistemas abertos [5,12]. No estudo realizado por Motti et al. [12], avaliando o número de contaminações e riscos de complicações infecciosas durante a diálise peritoneal, observou-se que 62% dos pacientes submetidos a sessões de diálises com sistemas abertos apresentaram infecções contra 23,3% em sistemas fechados.
O sistema desenvolvido é composto por coletor graduado e gotejador de soro do tipo microgotas, que servem para controlar o volume de infusão da solução de diálise ao abdome, visto que a infusão de líquido durante o procedimento ocasiona aumento pressórico abdominal, levando a repercussão no sistema cardiorrespiratório, principalmente em pacientes que apresentam baixo débito cardíaco [13].
O ponto autocicatrizante utilizado para injeções de medicamentos (Figura 1) permite a realização de correções de eletrólitos quando necessário, pois é sabido que durante o tratamento a criança pode apresentar distúrbios metabólicos [14].
A torneira de três vias utilizada para acoplar o sistema de diálise ao cateter é do tipo universal, ou seja, conecta-se a qualquer tipo de cateter para diálise, dispensando-se assim o uso de adaptadores, utilizado nos outros sistemas [11]. Uma das vias da torneira pode ser utilizada para coleta do líquido peritoneal ou para instalação do sistema de monitorização da pressão intra-abdominal (PIA). A mensuração da PIA é importante para avaliar a tolerância da infusão do dialisado, sendo recomendada a manutenção da pressão entre 5 e 15 cmH
2O [13].
O reservatório de drenagem graduado em 500 ml permite o armazenamento de maiores volumes, sem que haja a necessidade de descartes frequentes. O filtro de ar hidrófobo, na porção superior do reservatório, impede a contaminação do frasco pelo ar. O tubo de PVC que drena o fluido é protegido por uma tampa de segurança para esterilização e remoção do sistema da embalagem sem a contaminação da via distal. O conector tipo bico cego deve ser utilizado para conectar o tubo de PVC ao frasco caso ocorra perda da tampa de segurança, garantindo maior proteção ao sistema.
Para o uso clínico seguro dos sistemas de diálise peritoneal é fundamental garantir a esterilização do produto [15]. A eficácia do processo de esterilização foi comprovada pelos testes de esterilidade por inoculação indireta. Para que o teste tenha validade, a qualidade do ambiente de execução de ensaio, assim como os meios de cultura, a temperatura e o tempo de incubação são fatores importantes. Nos casos de esterilização por ETO, os indicadores biológicos e químicos acusam a difusão e a penetração do gás no interior do material, principalmente quando se trata de materiais plásticos complexos e embalagens múltiplas [16]. O gás é um eficaz agente esterilizante utilizado em artigos termossensíveis e apresenta boa penetração em embalagens e lúmens. Sua ação letal é atribuída à alquilação das cadeias protéicas microbianas, impedindo a multiplicação celular [15].
O desenvolvimento deste novo sistema de diálise peritoneal pediátrico fechado abre perspectivas para estudos clínicos, a fim de avaliar possíveis aplicações práticas futuras.
CONCLUSÃO
Foi possível desenvolver um novo sistema de diálise peritoneal pediátrico fechado de fácil manuseio e garantir sua esterilização, o que sugere sua aplicação clínica futura.
REFERÊNCIAS
1. Souza MH, Elias DO. Fundamentos da circulação extracorpórea. 2ª ed. Rio de Janeiro:Centro Editorial Alfa Rio; 2006.
2. Croti UA, Braile DM, Beani L, Fleury MCP. Monocúspide de homoenxerto decelularizado no tratamento do truncus arteriosus com a técnica de Barbero Marcial. Rev Bras Cir Cardiovasc. 2008;23(2):290-1. [MedLine] Visualizar artigo
3. Elias DO, Souza MHL, Lacerda BS, Fagundes FES, Lino FJS, Tiraboshi M. Injúria orgânica da circulação extracorpórea nos três primeiros meses de vida. Rev Bras Cir Cardiovasc. 1990;5(1):1-8. Visualizar artigo
4. Utley JR. Renal effects of cardiopulmonary bypass. In Utley JR. Pathophysiology and techniques of cardiopulmonary bypass. Baltimore:Williams & Wilkins;1982.
5. Guimarães RAC. Análise da implantação do sistema fechado simplificado durante a assistência de enfermagem aos clientes em diálise peritoneal intermitente manual. Rev Med Aeronaut Bras. 1993;43(1/2):10-9.
6. Calderón Elvir C, Duarte V, Juan C, Maza Vallejo J, Peralta Bustamante A. Uso y manejo del catéter de diálisis peritoneal permanente en pediatría. Acta Pediátr Méx. 1996;17(2):64-6.
7. Lima L, Mota C, Lira S, Faria M, Costa T, Pereira E. Peritonites em diálise peritoneal pediátrica. Rev Port Nefrol Hipert. 2005;19(2):103-10.
8. Noblat ACB, Mello ME, Leite EB, Luna MAC, Almeida ARP, Martinelli R. Peritonite por "B. subtilis" em diálise peritoneal intermitente, crônica. J Bras Nefrol. 1988;10(3):99-102.
9. Castro RP, Croti UA, Machado MN, Murillo HG, Rincon OYP, Policarpo SR, et al. Ultrafiltração convencional com modificação técnica no tratamento cirúrgico dos defeitos cardíacos congênitos. Rev Bras Cir Cardiovasc. 2006;21(1):42-9. Visualizar artigo
10. Cavagnaro FSM. Terapias continuas de reemplazo renal agudo en pediatría. Rev Chil Urol. 2003;68(2):125-30.
11. Fresenius medical care. Accessed in 21/01/2009. Avaliable from: URL: http://www.fmc-ag.com.br
12. Motti EF, Hutzler RU, Granato CF, Giorgi DM, Burdmann EA, Rodrigues E, et al. Contaminação bacteriana em diálise peritoneal, com sistema de drenagem aberto e fechado. J Bras Nefrol. 1982;4(3/4):69-72.
13. Barcellos PG, Johnston C, Carvalho WB, Fonseca MC, Santos JE, Bandini E. Repercussões cardiorrespiratórias da diálise peritoneal em crianças graves. RBTI. 2008;20(1):31-6.
14. Abensur H. Uso da diálise peritoneal em pacientes com insuficiência cardíaca congestiva. Rev Bras Hipertens. 2008;15(3):162-5.
15. Ramos EMN, Costa MFR, Oliveira OC, Ikeda T, Guimarães ZS. Central de material e esterilização. Manual técnico. Brasília; 2000.
16. Pinto TJA, Kaneko TM, Ohara MT. Controle biológico de qualidade de produtos farmacêuticos correlatos e cosméticos. 2ª ed. São Paulo: Atheneu; 2003. p.153-78.
CONFLITO DE INTERESSES:
Declaro haver conflito de interesse, pois o trabalho foi desenvolvido e financiado parcialmente pela empresa Braile Biomédica S/A®.
Article receive on sexta-feira, 2 de janeiro de 2009


 All scientific articles published at www.bjcvs.org are licensed under a Creative Commons license
All scientific articles published at www.bjcvs.org are licensed under a Creative Commons license