Estudar a viabilidade técnica e resultados imediatos da modificação técnica proposta por Caliani et al. para correção da coarctação aórtica com hipoplasia do arco aórtico.
Entre janeiro de 2005 e julho de 2006, nove neonatos com coarctação aórtica e hipoplasia do arco aórtico foram submetidos a uma nova abordagem cirúrgica para correção do defeito. A definição de hipoplasia do arco aórtico seguiu os critérios de Moulaert, segundo os quais o arco aórtico é considerado hipoplásico quando seu diâmetro atinge 50% do diâmetro da aorta ascendente. Nesta série, foram selecionados apenas pacientes com hipoplasia proximal e distal do arco aórtico. Várias técnicas foram propostas anteriormente, mas gradientes residuais importantes foram observados, assim como há o inconveniente da ligadura definitiva da artéria subclávia esquerda. A modificação técnica consiste em: toracotomia póstero-lateral esquerda, ampla mobilização da aorta descendente, com ligadura dos dois primeiros ramos intercostais, transecção da artéria subclávia esquerda em sua base, ressecção ampla de toda zona hipoplásica e adjacências do ducto arterioso, anastomose término-terminal entre o arco aórtico e aorta descendente com fio de PDS 7-0 e reimplante da artéria subclávia sobre a artéria carótida esquerda com anastomose látero-terminal.
Não houve óbito per-operatório ou tardio, o gradiente residual médio foi de 5 mmHg. Até o presente, não observamos nenhum caso de recoarctação ou de lesão neurológica medular.
A despeito do reduzido número de casos e do seguimento curto, esta modificação técnica pode representar uma excelente opção para tratamento deste complexo grupo de pacientes.
To study technical feasibility and early results of the technical modification suggested by Caliani et al. for correction of aortic coarctation and aortic arc.
Between January 2005 and July 2006, nine newborn patients with aortic coarctation and significant aortic hypoplasia were selected, and underwent a new surgical approach in order to correct this aortic defect. The definition of aortic arch hypoplasia according to Moulaert's criteria is an aortic arch with a diameter that is less than 50% of the diameter of the ascending aorta. In this study, only patients with proximal and distal aortic hypoplasia were selected. Many techniques were previously used, but significant residual gradients were observed, as well as the incovenience of definitive occlusion of the left subclavian artery. The aim of this study is to describe a new surgical technique that includes left posterolateral thoracotomy, wide mobilization of descending aorta with occlusion of the first two intercostal branches, transection of the left subclavian artery at its base, wide resection of the hypoplastic area and the surronding regions of the ductus arteriosus; end-to-end anastomosis between the aortic arch and descending aorta, with 7-0 PDS thread and reimplantation of the subclavian artery into the left carotid artery with side-to-end anastomosis.
There were no perioperative or late deaths. The mean residual gradient was 5 mmHg. Up to now, there were no cases of recoarctation or medullary neurological lesions.
Despite the small number of cases and the short follow-up, this technique modification may be an excellent option for the treatment of this complex situation.
INTRODUÇÃO
Coarctação aórtica é o estreitamento da aorta descendente, imediatamente abaixo da origem da artéria subclávia esquerda, em uma região denominada istmo, onde o ducto arterioso está conectado em contigüidade. Ela pode apresentar-se isoladamente, associada a anomalias intracardíacas e, ainda, com hipoplasia do arco aórtico.
As bases cirúrgicas da primeira correção de coarctação aórtica em neonato foram apresentadas por Mustard et al. [1], em 1953. Desde então, assistimos a uma melhora progressiva nos resultados. Entretanto, a correção de coarctação com hipoplasia do arco aórtico ainda representa um desafio para os cirurgiões [2].
A definição de hipoplasia do arco aórtico foi proposta por Moulaert et al. [3]. Ele é considerado hipoplásico quando seu diâmetro atinge 50% do diâmetro da aorta ascendente. A hipoplasia pode ser distal (ístmica - tipo A) ou proximal/distal (arco transverso - tipo B - Figura 1). Quando a coarctação aórtica associa-se à hipoplasia do arco, podemos inferir que se trata de cardiopatia ducto-dependente, onde na vida intra-uterina houve redução da perfusão desta região provocada por derivação sanguínea esquerda-direita que resultou no hipodesenvolvimento do arco e conseqüente migração de células ductais para a região ístmica [3].

Fig. 1 - Coarctação aórtica pré-ductal com hipoplasia do segmento aórtico entre as artérias carótida esquerda e subclávia esquerda
Estudos atuais demonstram que há consenso sobre a indicação de ampliação total do arco aórtico, mas não há consenso sobre qual técnica cirúrgica utilizar [2,4,5].
Progressos recentes nos cuidados intensivos dos neonatos e o afinamento das técnicas de eco-doppler bidimensional permitiram a correção de má formações intracardíacas complexas associadas a anomalias do arco aórtico em um único estágio, com resultados satisfatórios [6-8]. Nestes casos, a coarctação aórtica, associada ou não à hipoplasia do arco, é abordada cirurgicamente como interrupção do arco aórtico, utilizando-se circulação extracorpórea com hipotermia profunda e parada circulatória.
Outras técnicas foram descritas [4,9,10] para correção desta má formação, mas gradientes residuais importantes foram observados, recoarctações freqüentes e déficit de crescimento do membro superior esquerdo, notadamente quando o expediente de ligadura ou retalho da artéria subclávia é utilizado [4,11]. Soma-se a isso o denominador comum destas técnicas, que é a preservação da zona hipoplásica, cujo crescimento é restrito a longo prazo [12], podendo ocasionar retração.
O objetivo do presente trabalho é relatar uma nova técnica de correção de coarctação com hipoplasia do arco tipo B de Moulaert, que preserva os vasos da base, resseca a zona hipoplásica, ao mesmo tempo em que confere bom perfil hemodinâmico. Casos de coarctação ístmica isolada ou com hipoplasia tipo A não foram incluídos neste trabalho porque estas entidades patológicas podem ser tratadas com as técnicas convencionais de ressecção e anastomose término-terminal com bons resultados. A nosso ver, o verdadeiro desafio para o cirurgião reside na forma mais complexa, isto é, na hipoplasia tipo B.
MÉTODOS
Pacientes
Entre janeiro de 2005 e julho de 2006, nove neonatos com coarctação aórtica e hipoplasia do arco aórtico tipo B de Moulaert, internados em unidade de terapia intensiva, em uso de prostaglandina em infusão contínua objetivando a manutenção da permeabilidade do ducto arterioso, evoluindo com quadro de insuficiência cardíaca, hipertensão arterial e acidose metabólica, foram submetidos a correção cirúrgica com a técnica descrita a seguir. Três pacientes eram portadores de comunicação interventricular pequena. A idade dos pacientes variou de 3 a 20 dias, com média de 7 dias. Todos pacientes foram submetidos a ecocardiograma transtorácico previamente à operação. Nenhum estudo hemodinâmico foi realizado.
Técnica
A via de acesso em todos pacientes foi a toracotomia póstero-lateral esquerda. O pulmão esquerdo é afastado, a aorta descendente, ducto arterioso e vasos da base são amplamente dissecados até a aorta ascendente (Figura 2). O ducto arterioso é ligado com polipropilene 6-0 e os dois ou três primeiros ramos intercostais também, buscando ampla mobilidade da aorta descendente (Figuras 3 e 4). Uma dose de 0,5 mg/kg de heparina é administrada. Em seguida, procedemos ao pinçamento aórtico, que é feito logo após o tronco braquiocefálico e, na aorta descendente, após emergência do segundo ou terceiro ramo intercostal previamente ligado. As artérias carótida esquerda e subclávia são pinçadas. A artéria subclávia é então seccionada em sua base de implantação na aorta (Figura 5). O segmento distal permanece pinçado. A zona de coarctação e, sobretudo, o segmento hipoplásico, compreendido entre a artéria subclávia e carótida esquerda, são amplamente ressecados (Figura 6). Uma pequena abertura da concavidade do arco em direção à aorta ascendente é realizada, para se ampliar ao máximo a zona de anastomose. Na seqüência, uma anastomose término-terminal é feita entre o arco aórtico e aorta descendente com sutura contínua de PDS 7-0 (Figura 7).

Fig. 2 - Anatomia cirúrgica da coarctação aórtica com hipoplasia do arco

Fig. 3 - Ligadura das artérias intercostais

Fig. 4- Ligadura do ducto arterioso
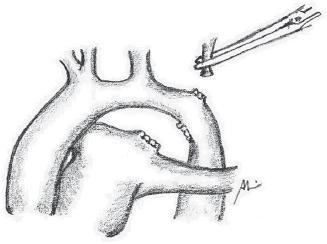
Fig. 5- Secção da artéria subclávia esquerda

Fig. 6- Ressecção ampla da zona de coarctação e do arco aórtico hipoplásico
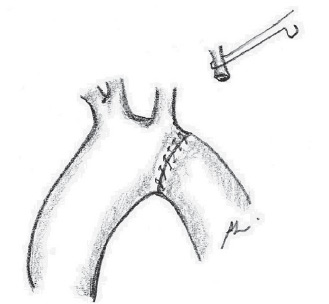
Fig. 7- Anastomose término-terminal entre a crossa e aorta descendente
As pinças são retiradas e a anastomose revisada. Procedemos, então, ao pinçamento parcial da artéria carótida esquerda em seu terço médio, onde faremos uma incisão vertical em sua parede. A artéria subclávia é reimplantada na artéria carótida mediante anastomose látero-terminal com sutura contínua de PDS 7-0 (Figura 8).

Fig. 8 - Reimplante da artéria subclávia em látero-terminal sobre a artéria carótida esquerda
Não houve mortalidade cirúrgica, acidente medular isquêmico ou seqüela neurológica advinda do pinçamento parcial da artéria carótida esquerda. O tempo de pinçamento aórtico foi de de 25 + 11 minutos.
A permanência hospitalar pós-operatória variou de 7 a 19 dias, com média de 11,7 + 1,1 dias.
Ecocardiograma doppler de controle, realizado na alta hospitalar e, 3 e 6 meses após a operação, evidenciou ausência de gradiente em seis pacientes (Figura 9) e gradiente residual de 10mmHg em três.
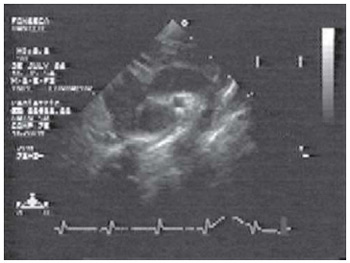
Fig. 9 - Eco-doppler de controle em paciente operado, mostrando arco aórtico após correção cirúrgica sem estenose residual
Todos pacientes são acompanhados clinicamente e até o presente momento não houve óbitos ou complicações tardias.
DISCUSSÃO
A incidência de hipoplasia do arco aórtico na coarctação varia de 65% a 81% [13]. A introdução da terapia com prostaglandinas no período neonatal modificou o histórico desta anomalia [9], com melhora significativa nos resultados. Estudos anatomopatológicos [14] e cirúrgicos [2,4,15] relatam a evidente obstrução gerada pela hipoplasia do arco aórtico.
Elevado porcentual de recoarctação em neonatos foi relatado após correção com anastomose término-terminal [16], flapping da artéria subclávia [11] e retalho de tecido sintético [17]. Mesmo a técnica de extensão da anastomose término-terminal [18-20] apresenta incidência superior a 10% de recoarctação.
Estudos histológicos confirmam a estrutura anormal do arco aórtico hipoplásico. Ela se caracteriza pelo elevado porcentual das fibras de colágeno em relação ao diâmetro da aorta e pela presença limitada de células alfa-actino-positivas, que são responsáveis pelo crescimento do vaso [12]. Isto reforça a teoria de que, para se obter um resultado satisfatório, a técnica cirúrgica deve contemplar a ressecção total da zona hipoplásica e do ducto arterioso.
Outras técnicas foram descritas [9,10] com aparentes bons resultados imediatos. Entretanto, ambas preservam a estrutura do arco aórtico hipoplásico, o que pode resultar em crescimento limitado ou retração da zona em torno da anastomose, causando recoarctação [12], ou sacrificam a artéria subclávia esquerda definitivamente com o conseqüente déficit de crescimento do membro superior esquerdo e suas conseqüências [13]. Outros autores preferem tratar esta anomalia como interrupção do arco aórtico, utilizando esternotomia, circulação extracorpórea e hipotermia profunda [8]. A nosso ver, este expediente não se faz necessário, exceto quando há anomalia intracardíaca associada que necessite correção em um só tempo.
Dentro da perspectiva de abordar a coarctação com hipoplasia do arco em todos seus aspectos, propomos uma técnica, sem circulação extracorpórea, que contempla as variáveis diretamente responsáveis pela alta incidência de recoarctações. Esta técnica está balizada nos seguintes princípios: 1) suprime totalmente o tecido ductal; 2) resseca a zona hipoplásica do arco e seus tecidos patológicos com baixo potencial de crescimento; 3) preserva a integridade dos vasos da base pelo reimplante da artéria subclávia esquerda; 4) não gera gradiente na anastomose.
CONCLUSÃO
Do ponto de vista técnico, acreditamos que a cirurgia que propomos só é factível com boa mobilização da aorta descendente. Isto pode ser obtido por meio da ampla dissecção e ligadura dos primeiros ramos intercostais. Caso contrário, nos parece difícil levar o segmento distal ao contato da base de implantação da artéria carótida esquerda e realizar anastomose término-terminal isenta de tensão. Na presente série, não deploramos acidentes ou seqüelas medulares isquêmicas, entretanto, este assunto nos questiona e ainda necessita de observação clínica complementar.
A despeito do reduzido número de casos e seguimento curto, esta modificação técnica, sem utilização de circulação extracorpórea e sem utilização de retalho sintético ou prótese, pode representar uma excelente opção para tratamento deste complexo grupo de pacientes e contribuir para a melhora dos resultados clínicos imediatos e a médio prazo.
REFERÊNCIAS
1. Diethrich EB, Ndiaye M, Reid DB. Stenting in the carotid artery: initial experience in 110 patients. J Endovasc Surg. 1996;3(1):42-62. [
MedLine]
2. Roubin GS, New G, Iyer SS, Vitek JJ, Al-Mubarak N, Liu MW, et al. Immediate and late clinical outcomes of carotid artery stenting in patients with symptomatic and asymptomatic carotid artery stenosis: a 5-year prospective analysis. Circulation. 2001;103(4):532-7. [
MedLine]
3. Hammer FD, Lacroix V, Duprez T, Grandin C, Verhelst R, Peeters A, et al. Cerebral microembolization after protected carotid artery stenting in surgical high-risk patients: results of a 2-year prospective study. J Vasc Surg. 2005;42(5):847-53.
4. Rapp JH, Wakil L, Sawhney R, Pan XM, Yenari MA, Glastonbury C, et al. Subclinical embolization after carotid artery stenting: new lesions on diffusion-weighted magnetic resonance imaging occur postprocedure. J Vasc Surg. 2007;45(5):867-72.
5. Piñero P, González A, Mayol A, Martínez E, González-Marcos JR, Boza F, et al. Silent ischemia after neuroprotected percutaneous carotid stenting: a diffusion-weighted MRI study. AJNR Am J Neuroradiol. 2006;27(6):1338-45. [
MedLine]
6. Faraglia V, Palombo G, Stella N, Taurino M, Iocca ML, Romano A, et al. Cerebral embolization in patients undergoing protected carotid-artery stenting and carotid surgey. J Cardiovasc Surg (Torino). 2007;48(6):683-8. [
MedLine]
7. Poppert H, Wolf O, Resch M, Theiss W, Schmidt-Thieme T, Graefin von Einsiedel H, et al. Differences in number, size and location of intracranial microembolic lesions after surgical versus endovascular treatment without protection device of carotid artery stenosis. J Neurol. 2004;251(10):1198-203. [
MedLine]
8. Schlüter M, Tübler T, Steffens JC, Mathey DG, Schofer J. Focal ischemia of the brain after neuroprotected carotid artery stenting. J Am Coll Cardiol. 2003;17:42(6):1007-13.
9. Mathur A, Roubin GS, Gomez CR, Iyer SS, Wong PM, Piamsomboon C, et al. Elective carotid artery stenting in the presence of contralateral occlusion. Am J Cardiol. 1998;81(11):1315-7. [
MedLine]
10. Perler BA, Dardik A, Burleyson GP, Gordon TA, Williams GM. Influence of age and hospital volume on the results of carotid endarterectomy: a statewide analysis of 9918 cases. J Vasc Surg. 1998;27(1):25-31. [
MedLine]
11. Hobson RW 2nd, Howard VJ, Roubin GS, Brott TG, Ferguson RD, Popma JJ, et al. Carotid artery stenting is associated with increased complications in octogenarians: 30-day stroke and death rates in the CREST lead-in phase. J Vasc Surg. 2004;(40):1106-11.
12. Sundt TM Jr, Ebersoldt MJ, Sharbrough FW, Piepgras DG, Marsh WR, Messick JM Jr, et al. The risk-benefit ratio of intraoperative shunting during carotid endarterectomy. Relevancy to operative and postoperative results and complications. Ann Surg. 1986;203(2):196-204. [
MedLine]
13. Riles TS. Surgical management of internal carotid artery stenosis: preventing complications. Can J Surg. 1994;37(2):124-7. [
MedLine]
14. Hertzer NR, O'Hara PJ, Mascha EJ, Krajewski LP, Sullivan TM, Beven EG. Early outcome assessment for 2228 consecutive carotid endarterectomy procedures: the Cleveland Clinic experience from 1989 to 1995. J Vasc Surg. 1997;26(1):1-10. [
MedLine]
15. CAVATAS investigators. Endovascular versus surgical treatment in patients with carotid stenosis in the Carotid and Vertebral Artery Transluminal Angioplasty Study (CAVATAS): a randomised trial. Lancet. 2001;357(9270):1729-37. [
MedLine]
16. Yadav JS, Wholey MH, Kuntz RE, Fayad P, Katzen BT, Mishkel GJ, et al. Protected carotid-artery stenting versus endarterectomy in high-risk patients. N Engl J Med. 2004;351(15):1493-501. [
MedLine]
17. SPACE Collaborative Group, Ringleb PA, Allenberg J, Brückmann H, Eckstein HH, Fraedrich G, Hartmann M, et al. 30 day results from the SPACE trial of stent-protected angioplasty versus carotid endarterectomy in symptomatic patients: a randomised non-inferiority trial. Lancet. 2006;368(9543):1239-47. [
MedLine]
18. Mozes G, Sullivan TM, Torres-Russotto DR, Bower TC, Hoskin TL, Sampaio SM, et al. Carotid endarterectomy in SAPPHIRE-eligible high-risk patients: implications for selecting patients for carotid angioplasty and stenting. J Vasc Surg. 2004;39(5):958-65.
19. Gasparis AP, Ricotta L, Cuadra SA, Char DJ, Purtill WA, Van Bemmelen PS, et al. High-risk carotid endarterectomy: fact or fiction. J Vasc Surg. 2003;37(1):40-6. [
MedLine]
20. Diethrich EB. Carotid endarterectomy is better than carotid stenting for asymptomatic patients. Pro position. Tex Heart Inst J. 2006;33(2):209-10. [
MedLine]
21. Diethrich EB. What happened to carotid stenting and will it be permanent? Anais Syllabus,CICE;2008.
22. Mas JL, Chatellier G, Beyssen B, Branchereau A, Moulin T, Becquemin JP, et al. Endarterectomy versus stenting in patients with symptomatic severe carotid stenosis. N Engl J Med. 2006;355(16):1660-71. [
MedLine]
23. Perler BA, Willians GM. Carotid endarterectomy in the very elderly: is it worthwhile? Surgery. 1994;116(3):479-83. [
MedLine]
24. O'Hara PJ, Hertzer NR, Mascha EJ, Beven EG, Krajewski LP, Sullivan TM. Carotid endarterectomy in octogenarians: early results and late outcome. J Vasc Surg. 1998;27(5):860-9.
25. Rockman CB, Jacobowitz GR, Adelman MA, Lamparello PJ, Cagne PJ, Landis R, et al. The benefits of carotid endarterectomy in the octogenarian: a challenge to the resuts of carotid angioplasty and stenting. Ann Vasc Surg. 2003;17(1):9-14. [
MedLine]
26. Bonamigo TP, Lucas ML. Análise crítica das indicações e resultados do tratamento cirúrgico da doença carotídea. J Vasc Bras. 2007;6(4):366-77.
27. European Carotid Surgery Trialists' Collaborative Group. MRC European Carotid Surgery Trial: interim results for symptomatic patients with severe (70-99%) or with mild (029%) carotid stenosis. Lancet. 1991;337(8752):1235-43. [
MedLine]
28. Bonamigo TP, Weber EL, Lucas ML, Bianco C, Cardozo MA. Carotid endarterectomy in patients with contralateral occlusion: a 10-year experience. J Vasc Bras. 2004;3(1):83-91.
29. Samson RH, Showalter DP, Yunis JP. Routine carotid endarterectomy without a shunt, even in the presence of a contralateral occlusion. Cardiovasc Surg. 1998;6(5):475-84. [
MedLine]









 All scientific articles published at www.bjcvs.org are licensed under a Creative Commons license
All scientific articles published at www.bjcvs.org are licensed under a Creative Commons license