INTRODUÇÃO
Atenção crescente vem sendo dada, nas últimas décadas, ao papel da inflamação na aterosclerose. O processo inflamatório pode modular a ruptura da placa (e, conseqüentemente, a trombose) e o remodelamento [1]. Nos aneurismas de aorta abdominal (AAA), comumente causados pela aterosclerose, a destruição de componentes da matriz extracelular, em particular de tecido elástico, é considerada mecanismo de extrema importância, influenciando a perda da rigidez normal da parede e sua dilatação. Essa destruição pode ser induzida por proteases da matriz, incluindo-se a elastase [2]; células inflamatórias são a principal fonte de tais enzimas. Variação individual na resposta inflamatória poderia ser uma explicação para o fato de que, ainda que a aterosclerose seja doença freqüente, os aneurismas sejam complicação relativamente incomum - apenas casos de aterosclerose com infiltrado inflamatório proeminente apresentariam esse tipo de remodelamento arterial.
Em paralelo à importância dada à inflamação, há diversos estudos tentando revelar seus fatores causais, enfocando essencialmente na pesquisa de agentes infecciosos que possam estar envolvidos na aterosclerose. Entre outros [3], a Chlamydia pneumoniae recebeu a atenção de diversos autores que acreditam em um papel de agentes infecciosos nessa doença, nas artérias coronárias inclusive. Neste território arterial, estudos prévios de nosso laboratório revelaram a presença não só desse tipo de bactéria, mas também de Mycoplasma pneumoniae [4-7]. Tais estudos encontraram Mycoplasma pneumoniae em quase todos os ateromas, mas uma grande quantidade de ambas as bactérias pareceu fundamental para o desenvolvimento de instabilidade da placa. É sabido que a co-infecção de M. pneumoniae com outra bactéria potencializa a virulência de ambos os agentes infecciosos [8,9].
O fato de que o micoplasma requer colesterol para sobreviver, pois sua membrana tem esse tipo de gordura em sua constituição, propriedade única entre os procariontes, está em acordo com os achados desses microorganismos na aterosclerose. Foi também previamente mostrado que as placas ateroscleróticas trombosadas estão associadas a remodelamento positivo [10,11]. Os aneurismas da aorta podem ser considerados um remodelamento vascular positivo segmentar, e são acompanhados de trombose em placas gordurosas ulceradas - em outras palavras, processo com características semelhantes às lesões coronárias vulneráveis.
A associação entre Chlamydia pneumoniae e aneurismas abdominais aórticos foi investigada por diversos autores, que demonstraram graus variáveis de correlação que poderiam indicar eventual papel causal dessas bactérias em tal doença [12-17]. No entanto, os estudos morfológicos, sejam por microscopia eletrônica, por imuno-histoquímica ou por hibridização in situ, apenas detectaram o agente, sem quantificá-lo. Por outro lado, a presença de Mycoplasma pneumoniae nessas lesões foi menos investigada; dados obtidos por meio da técnica da reação em cadeia da polimerase (polimerase chain reaction, PCR), não indicam a ligação dessa bactéria com a afecção aórtica [16,18].
O objetivo do presente estudo é verificar se esses dois agentes estão presentes nos AAA, usando outra abordagem para a detecção de M. pneumoniae, e se sua quantidade é maior em aneurismas em comparação com áreas de aterosclerose sem tal complicação.
MÉTODO
O presente estudo foi aprovado pela Comissão Científica e de Ética do Instituto do Coração (InCor) do Hospital das Clínicas da Universidade de São Paulo.
Pacientes
Cortes transversais de 10 aneurismas ateroscleróticos de aorta abdominal situados entre a origem das artérias renais e a bifurcação aórtica, selecionados ao acaso entre as necropsias realizadas no Laboratório de Anatomia Patológica do Instituto do Coração (InCor) do Hospital das Clínicas da Universidade de São Paulo, em São Paulo, Brasil, foram incluídos no estudo. Tais necropsias foram realizadas sempre dentro de um período de, no máximo, 24 horas, na maior parte das vezes igual ou inferior a 12 horas, após a morte dos pacientes. Estes morreram em decorrência de ruptura do aneurisma (dois casos) ou de doença isquêmica do coração; em um paciente, esta era associada a doença reumática e endocardite infecciosa. Só foram usadas artérias de adultos. Casos em que a aorta abdominal tivesse qualquer outro processo patológico, tal como dissecção, foram excluídos.
Foram feitos três grupos-controle. O primeiro corresponde às mesmas aortas abdominais dos casos, fora do aneurisma, desde que a dilatação não tomasse toda a porção sub-renal da artéria (denominamos esse grupo de "atero-aneu"). Amostras de aortas abdominais de 10 pacientes com aterosclerose grave, porém sem aneurismas, constituíram o segundo grupo-controle; um dos casos apresentava dissecção da aorta ascendente, mas a descendente (abdominal inclusive) estava livre de comprometimento por esta doença. O terceiro grupo-controle foi composto por amostras de 10 aortas abdominais que eram normais ou tinham aterosclerose leve (tipos I a II pela classificação da American Heart Association).
Método
Após fixação em formol, os fragmentos, com exceção dos normais, foram descalcificados em solução aquosa de 100d de ácido trissódico e 250mL de ácido fórmico/L, durante 4 a 6 dias. Após isso, foram submetidos a processamento histológico de rotina e embebidos em parafina. Cortes com 3 mm de espessura foram utilizados para coloração pela hematoxilina e eosina (HE), pelo método de Verhoeff (sem contracoloração para colágeno) para salientar as fibras elásticas e assim delimitar as camadas vasculares, e para reações de imunoperoxidase para detecção de Chlamydia pneumoniae. Para revelação de Micoplasma pneumoniae, reações de hibridização in situ foram efetuadas em cortes com 5 mm de espessura.
As lâminas coradas pelo HE foram usadas para avaliação geral das lesões e para escolher o corte e a área, com cerca de 1 cm, na qual o vaso estivesse mais preservado e pudesse ser melhor analisado; as reações para C. pneumoniae e M. pneumoniae foram preparadas nessas regiões.
Determinação da espessura das túnicas íntima e média - Essas medidas foram feitas nas lâminas coradas pelo método de Verhoeff, com utilização de programa computadorizado de análise de imagens (Quantimet 500) acoplado a microscópio usando a objetiva de 10x. Essa espessura foi medida no meio e nas bordas dos cortes; a medida considerada para cada vaso foi a média desses três valores. Em alguns casos, considerou-se que havia placas ateroscleróticas que mudavam substancialmente essa média e que não haviam sido incluídas nas três medidas acima. Nesses casos, a espessura dessa área foi também computada como quarta medida.
Quantificação das fibras elásticas- Nas mesmas lâminas coradas pelo Verhoeff, e com o mesmo sistema óptico usado para a determinação da espessura das camadas, foi medida, tanto na média quanto na adventícia, e em toda a extensão do corte, a porcentagem de área positiva para fibras elásticas por micrômetro quadrado.
Quantificação of Chlamydia pneumoniae - Reações de imunoperoxidase foram realizadas para essa quantificação. Anticorpo monoclonal para proteína predominante na membrana externa de C. pneumoniae (Dako, Dinamarca, clone RR-402) foi usado sem diluição como anticorpo primário, com incubação por aproximadamente 16 horas ("overnight") a 4oC, após recuperação antigênica induzida por calor em forno de microondas (em tampão citrato 0,01M por 10 minutos), bloqueio da peroxidase endógena com H2O2 a 3% em tampão TRIS durante dois períodos de 10 minutos cada, e inibição de coloração inespecífica por incubação com soro fetal bovino não-imune diluído em solução de tampão fosfato (PBS) por uma hora em câmara a 37oC. O anticorpo secundário também foi fornecido pela firma Dako, da Dinamarca (E-354). Conjugados peroxidase-estreptoavidina (Amersham, Reino Unido) e diaminobenzidina (DAB, Dako, Estados Unidos da América) foram usados para revelação, e hematoxilina de Harris para contracoloração.
O número de células positivas para C. pneumoniae por micrômetro quadrado foi contado em cada camada de cada artéria, na extensão de um centímetro. A área foi medida no mesmo sistema computadorizado de análise de imagens (Quantimet 500), acoplado ao microscópio usando a objetiva de 10x. Ainda que tenha sido buscada uma otimização da coincidência entre a imagem ao microscópio e à tela do computador, foi impossível evitar que a cor castanha, correspondente à positividade, fosse um pouco mais exuberante na tela. Assim, o observador teve que ser bastante restritivo durante a contagem. De todo modo, essa dificuldade foi similar em todos os casos; se houve algum erro, foi sistemático, e provavelmente não influenciou a comparação entre os grupos.
Quantificação de Mycoplasma pneumoniae - Para as reações de hibridização in situ, os cortes foram aquecidos em banho-maria durante 45 minutos, submetidos a bloqueio de peroxidase semelhante ao usado na técnica da imuno-histoquímica, imersos em bloqueio protéico sem soro (Dako, Dinamarca), durante 15 minutos, e a seguir incubados com 20 mL de sonda biotinilada para M. pneumoniae para cada 80 mL de solução contendo formamida deionizada a 50%, sulfato de dextrana, tampão de citrato de sódio 20x, solução de Denhardt, ácido desoxirribonucléico de esperma de salmão, ácido ribonucléico de transferência de fungos, poli-A e poli-C e água bidestilada, inicialmente a 95oC, durante 6 minutos, e depois em câmara úmida a 37oC, durante cerca de 16 horas ("overnight"). O sinal foi desenvolvido e amplificado com o sistema GenPoint, e DAB usado para revelação, com contracoloração com hematoxilina de Harris. Após os cortes terem sido assim preparados, foram analisados no mesmo sistema computadorizado descrito acima, e a porcentagem de área positiva para M. pneumoniae foi calculada, também em cada camada de cada artéria, no comprimento de um centímetro. Aplicam-se as mesmas considerações feitas no tópico anterior a respeito de dissimilaridades entre imagens no microscópio e na tela.
Análise estatística
Como os dados envolvem tanto grupos pareados (áreas dentro e fora dos aneurismas nos casos) como não-pareados (os dois outros grupos-controle), a avaliação dos resultados foi planejada para ser feita usando o teste de Wald. No entanto, como a distribuição dos valores não foi normal, foi feito ranqueamento dos casos para cada variável; a análise foi então aplicada considerando-se a posição no ranqueamento como variável (cuja adesão à normalidade foi positiva) a ser testada [19].
O nível de significância foi estabelecido em 5% e o sistema SAS® usado para os cálculos estatísticos.
RESULTADOS
Idade, gênero e doença principal e/ou causa de morte dos pacientes envolvidos na investigação são apresentados na Tabela 1. Exemplos de cortes corados com Verhoeff e submetidos a reações para Chlamydia pneumoniae e Mycoplasma pneumoniae são mostrados nas Figuras 1 a 3.


Fig 1 - Coloração para sistema elástico nas aortas abdominais. A- paciente sem aterosclerose significativa (normal); B- paciente com aterosclerose, sem aneurismas; C e D- paciente com aneurisma, em área fora (C) ou dentro dele (D). PA - placa aterosclerótica; T- trombo. Coloração pelo método de Verhoeff, aumento da objetiva 5x

Fig. 2 - Imuno-histoquímica para C. pneumoniae na íntima (A), média (B) e adventícia (C) de uma aorta sem aterosclerose significativa. D- mesma reação em uma placa aterosclerótica dentro de um aneurisma. As células positivas estão coradas em castanho. As setas apontam alguns dos cristais de colesterol situados dentro das placas. Aumento da objetiva 40x

Fig. 3 - Hibridização "in situ" para M. pneumoniae na íntima (A), média (B) e adventícia (C) de uma aorta sem aterosclerose significativa. D- mesma reação em uma placa aterosclerótica dentro de um aneurisma. As células positivas estão coradas em castanho. As setas apontam alguns dos cristais de colesterol situados dentro das placas. Aumento da objetiva 40x
Como a análise estatística foi feita tomando em consideração a ordem (ranqueamento) de cada medida, as tabelas mostram a posição média de cada grupo, além das medianas, médias e desvios-padrão. Para facilitar o reconhecimento visual dos resultados, os gráficos concernentes às espessuras da íntima e da média e à porcentagem de tecido elástico foram elaborados tomando em consideração as médias.
A Tabela 2 e a Figura 4 mostram a espessura das túnicas íntima e média em cada grupo. As regiões aneurismáticas apresentavam as íntimas mais espessas e as aortas normais as mais finas. As lesões ateroscleróticas não-aneurismáticas, nos casos com e sem aneurismas, ocupavam posição intermediária. No entanto, foi encontrada diferença significativa entre o grupo normal e os outros três (normal vs. aneurismas, normal vs. atero/aneu, normal vs. aterosclerose, todos p< 0,01), mas não nestes últimos entre si (aneurismas vs. atero/aneu, p=0,12; aneurismas vs. aterosclerose, p=0,35; atero/aneu vs. aterosclerose, p=0,36). Em contraste, as aortas normais tinham as médias mais espessas e as aneurismáticas as mais finas; uma vez mais, as medidas das lesões ateroscleróticas não-aneurismáticas ficaram entre as dos outros grupos. Com relação a essa camada, os dois grupos de aterosclerose sem aneurisma (atero/aneu e aterosclerose) foram similares entre si (p=0,89), mas as regiões com os aneurismas eram significativamente mais finas, e as artérias normais mais espessas que os outros grupos (todos p<0,01). A Figura 5 mostra a quantidade de tecido elástico na média e na adventícia. As áreas com aneurismas tinham os menores valores, em comparação tanto com a mesma artéria, fora deles (p<0,01), quanto com as aortas de outros pacientes com (p<0,01) ou sem aterosclerose (p=0,04). Por outro lado, não foi encontrada diferença entre atero/aneu e aterosclerose (p=0,40), indicando que a destruição do tecido elástico não está relacionada à aterosclerose, mas aos aneurismas.
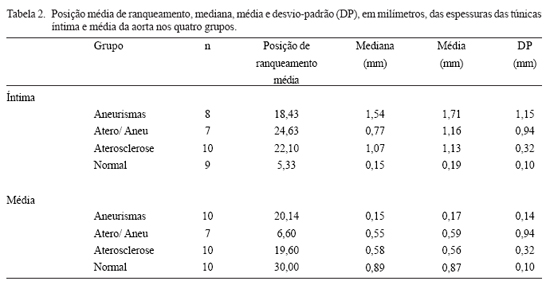
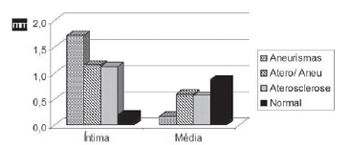
Fig. 4 - Espessura média das camadas da aorta abdominal em áreas aneurismáticas (aneurismas), em pacientes com aneurismas, em áreas fora da lesão (atero/ aneu), em pacientes com aterosclerose, mas sem aneurismas (aterosclerose), e em pacientes sem aterosclerose significativa (normal)
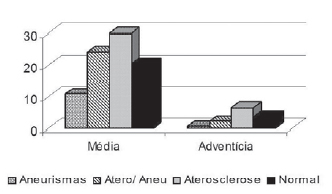
Fig. 5 - Porcentagem média de tecido elástico na média e na adventícia da aorta abdominal em áreas aneurismáticas (aneurismas), em pacientes com aneurismas, em áreas fora da lesão (atero/ aneu), em pacientes com aterosclerose, mas sem aneurismas (aterosclerose), e em pacientes sem aterosclerose significativa (normal)
Os resultados sobre o número de células positivas para C. pneumoniae são apresentados na Tabela 3 e na Figura 6. O achado dessas bactérias foi mais freqüente na adventícia, em todos os grupos; nenhuma diferença significativa foi encontrada entre eles (todos p>0,05).
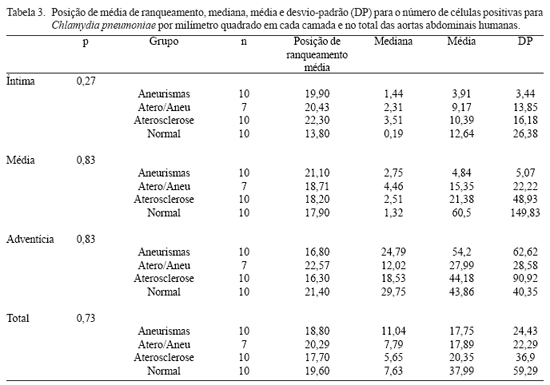
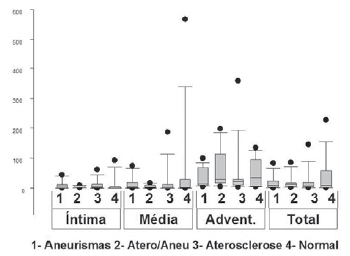
Fig. 6 - Gráfico do tipo "box-plot" do número de células positivas para C. pneumoniae nas camadas íntima, média e adventícia, e no total do vaso, em aorta abdominal em áreas aneurismáticas (1- aneurismas), em pacientes com aneurismas, em áreas fora da lesão (2- atero/ aneu), em pacientes com aterosclerose, mas sem aneurismas (3- aterosclerose), e em pacientes sem aterosclerose significativa (4- normal)
A Tabela 4 e a Figura 7 mostram a porcentagem de área ocupada por M. pneumoniae em cada grupo. O grupo de pacientes com aterosclerose, mas sem aneurisma, foi no qual este agente predominava, seja na íntima, seja na adventícia, mas as diferenças não foram significativas (todos p>0,05).
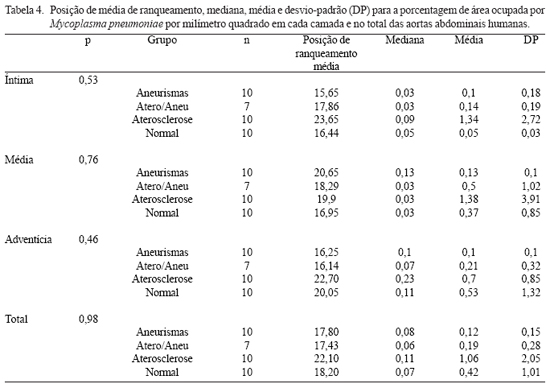
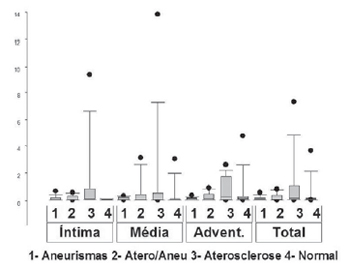
Fig. 7 - Gráfico do tipo "box-plot" da porcentagem de área ocupada por M. pneumoniae nas camadas íntima, média e adventícia, e no total do vaso, em aorta abdominal em áreas aneurismáticas (1- aneurismas), em pacientes com aneurismas, em áreas fora da lesão (2- atero/ aneu), em pacientes com aterosclerose, mas sem aneurismas (3- aterosclerose), e em pacientes sem aterosclerose significativa (4- normal)
Tentando obter um quadro o mais completo possível com relação a putativo envolvimento de Chlamydia pneumoniae e/ou Mycoplasma pneumoniae na patogênese da aterosclerose e dos aneurismas da aorta abdominal, nós usamos três tipos de controles: 1) as mesmas aortas abdominais que constituíram o grupo de estudo, fora da área de aneurisma. Esse controle foi incluído para eventualmente revelar alterações localizadas que pudessem explicar porque uma área específica sofre dilatação, mas não o restante do vaso. Esse grupo controle tinha apenas 7 casos porque 3 aneurismas tomavam toda a aorta abdominal; 2) aortas com aterosclerose grave, sem aneurismas. Como apenas pequena porcentagem dos pacientes com aterosclerose grave desenvolve aneurismas, o objetivo dessa comparação era procurar fatores que pudessem distinguir esses pacientes da maioria; 3) aortas sem aterosclerose significativa foram incluídas como verdadeiros controles, em especial para verificar a possibilidade da presença das bactérias enfocadas mesmo em pessoas normais.
A avaliação de idade e gênero dos pacientes não era objetivo do presente estudo. Como esperado, as idades dos casos com aterosclerose (com ou sem aneurismas) eram maiores que aquelas do grupo normal. Uma proporção maior de homens entre os casos de aneurisma também podia ser antecipada de acordo com dados epidemiológicos [20], ainda que tenhamos tido 90% desse gênero, enquanto na literatura a preponderância não chega a ser tão alta, variando, conforme a revisão, entre 66% e 81% [20]. Também tivemos número relativamente alto de mulheres nos grupos controles, com e sem aterosclerose.
Os resultados sobre a espessura das camadas aórticas estiveram em acordo com a expectativa: aortas normais tinham as íntimas mais finas e as médias mais grossas, o oposto ocorrendo com os aneurismas. Considerando que a aterosclerose é um acúmulo intimal de lípides e outros materiais, é fácil entender porque os três grupos de segmentos aórticos com aterosclerose tinham íntima maior; as diferenças entre lesões ateroscleróticas com e sem aneurisma não foram significativas. Por outro lado, afilamento da média é efeito secundário bem conhecido da aterosclerose; a destruição do tecido elástico que está associada ao estabelecimento dos aneurismas faz com que tal característica seja particularmente exuberante. Esses fatos explicam porque a média era mais fina nos aneurismas, intermediária nas áreas ateroscleróticas fora deles (independentemente da presença ou não da dilatação da artéria) e mais grossa nas aortas sem aterosclerose.
Detectamos Chlamydia pneumoniae e Mycoplasma pneumoniae em todos os grupos. Pesquisa anterior de Mycoplasma pneumoniae em AAA, usando o método da reação de polimerase em cadeia (PCR), resultou negativa. Com relação à Chamydia pneumoniae, os achados prévios são controversos: a porcentagem de casos positivos varia de 0% a 100%, seja por PCR [21], hibridização in situ, ou imuno-histoquímica.
Tal variação entre os dados de diferentes centros e a presença das bactérias em todos os nossos grupos levanta a questão de se as reações poderiam mostrar falso positivo. Foi sugerido que os anticorpos contra a membrana de Chlamydia pneumoniae, usados nas reações de imunoperoxidase (assim como em Western blots, que não realizamos), poderiam ter reação cruzada com cadeia de hemoglobina b [22] ou cadeias pesadas de imunoglobulinas [23] e, desse modo, constituir resultado inespecífico. Esses estudos, porém, utilizaram anticorpos preparados por seus próprios autores, em lugar do anticorpo comercial usado por nós e pela maioria dos pesquisadores, ainda que direcionados à mesma membrana externa da clamídia.
Os estudos que enfocaram AAA não mediram comparativamente o grau de infecção dos pacientes. Por outro lado, como descrevemos nas aortas, pesquisas prévias de nosso laboratório mostraram que mesmo pessoas sem aterosclerose podem apresentar alguma quantidade dessas bactérias em artéria coronárias. Nesse território arterial, foram demonstradas diferenças significantes entre grupos com e sem aterosclerose e entre placas estáveis e instáveis [4-7]. Esses pontos fortalecem a necessidade de método quantitativo para melhor analisar o papel da clamídia e do micoplasma nas doenças.
Usando método quantitativo, no presente artigo, não mostramos qualquer diferença entre os grupos com respeito a nenhum dos dois tipos de microorganismos, diferentemente do que nosso laboratório descreveu nas artérias coronárias. Uma possível explicação para esse fato poderia envolver a população incluída nos estudos. Nos outros artigos, apenas artérias coronárias de pacientes com miocardiopatia dilatada idiopática ou doença de Chagas entraram no grupo controle [4-7], enquanto neste trabalho, entre os pacientes sem aterosclerose aórtica incluídos havia casos de transplante cardíaco, doenças infecciosas, neoplasia e doença reumática (Tabela 1); um dos casos de aneurisma também tinha doença reumática e endocardite infecciosa. É possível que esses casos causem ou sejam causados por algum tipo de desbalanço imunológico, que poderia interferir com a capacidade dos pacientes reagirem às bactérias que enfocamos, influenciando assim nossos resultados. Essa idéia é reforçada pela observação de que pacientes chagásicos apresentam menos micoplasma e clamídia em seus tecidos [24], o que aumentaria ainda mais as diferenças entre as populações controle dos dois estudos.
Algumas das diferenças observadas nas artérias coronárias foram detectadas em número de pacientes semelhante ao do presente trabalho [4]. No entanto, o tamanho relativamente pequeno da nossa amostra diminui o poder estatístico da comparação, não se podendo descartar por completo a possibilidade de que diferença real entre os grupos tenha ficado encoberta por esse motivo.
Já foram descritas outras diferenças no processo aterosclerótico entre a aorta e as artérias coronárias, além da aparente ausência de papel dessas bactérias no processo, que contrasta com os estudos pregressos deste laboratório. Enquanto nas artérias coronárias as estrias lipoídicas e placas ateroscleróticas têm a mesma distribuição, nas aortas, esses dois tipos de lesão aterosclerótica têm localizações dissimilares [25]. O tempo de surgimento e evolução é diferente - na aorta, o processo começa na infância, e progride em ritmo lento, enquanto nas artérias coronárias as lesões começam na puberdade [26]. O conteúdo lipídico das lesões também varia conforme o território vascular, ao menos nas estrias lipoídicas [27]. Até mesmo na própria aorta a distribuição não é homogênea: o acometimento da porção abdominal é muito mais grave que o do segmento torácico. Em outro artigo realizado por nosso grupo, encontramos correlação entre intensidade de lesões ateroscleróticas e diâmetro vascular na aorta torácica, mas não na abdominal [28]. Assim sendo, as diferenças relativas a Chlamydia pneumoniae e Mycoplasma pneumoniae entre os dois leitos arteriais pode também representar uma real distinção entre o processo aterosclerótico nos dois territórios. De todo modo, nossos dados sugerem que os agentes enfocados não parecem ter papel importante na patogênese dos AAA.
AGRADECIMENTOS
Este estudo foi financiado pela Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP), Brasil, processos números 99/00322-9 e 01/06917-6. Os autores agradecem a Adriana Psota, Solange A. Consorti, Joana P. Araújo, Sueli A. P. Salomino e Nádia V. Sambiase por seu apoio na preparação de lâminas e reações de imuno-histoquímica e hibridização in situ.
REFERÊNCIAS
1. Faxon DP, Fuster V, Libby P, Beckman JA, Hiatt WR, Thompson RW, et al. Atherosclerotic Vascular Disease Conference: Writing Group III: pathophysiology. American Heart Association. Circulation. 2004;109(21):2617-25. [
MedLine]
2. Shah PK. Inflammation, metalloproteinases, and increased proteolysis: an emerging pathophysiological paradigm in aortic aneurysm. Circulation. 1997;96(7):2115-7. [
MedLine]
3. Marques da Silva R, Lingaas PS, Geiran O, Tronstad L, Olsen I. Multiple bacteria in aortic aneurysms. J Vasc Surg. 2003;38(6):1384-9. [
MedLine]
4. Higuchi M, Castelli JB, Aiello VD, Palomino S, Reis MM, Sambiase NV, et al. Great amount of C. pneumoniae in ruptured plaque vessel segments at autopsy: a comparative study with stable plaques. Arq Bras Cardiol. 2000;74(2):149-51. [
MedLine]
5. Higuchi ML, Sambiase N, Palomino S, Gutierrez P, Demarchi LM, Aiello VD, et al. Detection of Mycoplasma pneumoniae and Chlamydia pneumoniae in ruptured atherosclerotic plaques. Braz J Med Biol Res. 2000;33(9):1023-6. [
MedLine]
6. Higuchi M de L, Ramires JA. Infectious agents in coronary atheromas: a possible role in the pathogenesis of plaque rupture and acute myocardial infarction. Rev Inst Med Trop São Paulo. 2002;44(4):217-24. [
MedLine]
7. Higuchi M de L, Reis MM, Sambiase NV, Palomino SA, Castelli JB, Gutierrez PS, et al. Coinfection with Mycoplasma pneumoniae and Chlamydia pneumoniae in ruptured plaques associated with acute myocardial infarction. Arq Bras Cardiol. 2003;81(1):12-22. [
MedLine]
8. Stacey A, Bradlow A. Arcanobacterium haemolyticum and Mycoplasma pneumoniae co-infection. J Infection. 1999;38(1):41-2.
9. Razin S, Yogev D, Naot Y. Molecular biology and pathogenicity of mycoplasmas. Microbiol Mol Biol Rev. 1998;62(4):1094-156.
10. Bezerra HG, Higuchi ML, Gutierrez PS, Palomino SA, Silvestre JM, Libby P, et al. Atheromas that cause fatal thrombosis are usually large and frequently accompanied by vessel enlargement. Cardiovasc Pathol. 2001;10(4):189-96. [
MedLine]
11. Pasterkamp G, Schoneveld AH, van Wolferen W, Hillen B, Clarijs RJ, Haudenschild CC, et al. The impact of atherosclerotic arterial remodeling on percentage of luminal stenosis varies widely within the arterial system: a postmortem study. Arterioscler Thromb Vasc Biol. 1997;17(11):3057-63. [
MedLine]
12. Blasi F, Denti F, Erba M, Cosentini R, Raccanelli R, Rinaldi A, et al. Detection of Chlamydia pneumoniae but not Helicobacter pylori in atherosclerotic plaques of aortic aneurysms. J Clin Microbiol. 1996;34(11):2766-9. [
MedLine]
13. Juvonen J, Juvonen T, Laurila A, Alakarppa H, Lounatmaa K, Surcel HM, et al. Immunohistochemical detection of Chlamydia pneumoniae in abdominal aortic aneurysms. Ann N Y Acad Sci. 1996;800:236-8. [
MedLine]
14. Lindholt JS, Ostergard L, Henneberg EW, Fasting H, Andersen P. Failure to demonstrate Chlamydia pneumoniae in symptomatic abdominal aortic aneurysms by a nested polymerase chain reaction (PCR). Eur J Vasc Endovasc Surg. 1998;15(2):161-4. [
MedLine]
15. Karlsson L, Gnarpe J, Naas J, Olsson G, Lindholm J, Steen B, et al. Detection of viable Chlamydia pneumoniae in abdominal aortic aneurysms. Eur J Vasc Endovasc Surg. 2000;19(6):630-5. [
MedLine]
16. Maraha B, Berg H, Scheffer GJ, van der Zee A, Bergmans A, Misere J, et al. Correlation between detection methods of Chlamydia pneumoniae in atherosclerotic and non-atherosclerotic tissues. Diagn Microbiol Infect Dis. 2001;39(3):139-43. [
MedLine]
17. Porqueddu M, Spirito R, Parolari A, Zanobini M, Pompilio G, Polvani G, et al. Lack of association between serum immunoreactivity and Chlamydia pneumoniae detection in the human aortic wall. Circulation. 2002;106(21):2647-8. [
MedLine]
18. Blasi F, Boman J, Esposito G, Melissano G, Chiesa R, Cosentini R, et al. Chlamydia pneumoniae DNA detection in peripheral blood mononuclear cells is predictive of vascular infection. J Infect Dis. 1999;180(6):2074-6. [
MedLine]
19. Agresti A. Categorical data analysis. New York:John Wiley & Sons;1990. p.461.
20. Harthun NL, Cheanvechai V, Graham LM, Freischlag JA, Gahtan V. Prevalence of abdominal aortic aneurysm and repair outcomes on the basis of patient sex: should the timing of intervention be the same? J Thorac Cardiovasc Surg. 2004;127(2):325-8. [
MedLine]
21. Apfalter P, Blasi F, Boman J, Gaydos CA, Kundi M, Maass M, et al. Multicenter comparison trial of DNA extraction methods and PCR assays for detection of Chlamydia pneumoniae in endarterectomy specimens. J Clin Microbiol. 2001;39(2):519-24. [
MedLine]
22. Vammen S, Vorum H, Ostergaard L, Henneberg EW, Lindholt JS. Immunoblotting analysis of abdominal aortic aneurysms using antibodies against Chlamydia pneumoniae recombinant MOMP. Eur J Vasc Endovasc Surg. 2002;24(1):81-5. [
MedLine]
23. Lindholt JS, Stovring J, Ostergaard L, Urbonavicius S, Henneberg EW, Honore B, et al. Serum antibodies against Chlamydia pneumoniae outer membrane protein cross-react with the heavy chain of immunoglobulin in the wall of abdominal aortic aneurysms. Circulation. 2004;109(17):2097-102. [
MedLine]
24. Higuchi ML. Trypanosoma cruzi trans-sialidase as a new therapeutic tool in the treatment of chronic inflammatory diseases: possible action against mycoplasma and chlamydia. Med Hypotheses. 2004;63:616-23. [
MedLine]
25. McGill HC Jr. General findings of the International Project of Atherosclerosis. Lab Invest. 1968;18(5):498-502. [
MedLine]
26. McGill HC Jr. Fatty streaks in the coronary arteries and aorta. Lab Invest. 1968;18(5):560-4. [
MedLine]
27. Panganamala RV, Geer JC, Sharma HM, Cornwell DG. The gross and histologic appearance and the lipid composition of normal intima and lesions from human coronary arteries and aorta. Atherosclerosis. 1974;20(1):93-104. [
MedLine]
28. Benvenuti LA, Onishi RY, Gutierrez PS, Higuchi ML. Different patterns of atherosclerotic remodeling in the thoracic and abdominal aorta. Clinics. 2005;60(5):355-60. [
MedLine]











 All scientific articles published at www.bjcvs.org are licensed under a Creative Commons license
All scientific articles published at www.bjcvs.org are licensed under a Creative Commons license